09/02/2021
Un avis de l’Efsa sur l’usage des insectes en alimentation humaine
En janvier 2021, l’Agence européenne de sécurité alimentaire (Efsa) a publié un avis autorisant l’utilisation d’insectes en alimentation humaine, dans le cadre du règlement novel food. Ce faisant, l’Efsa répond à une demande de la Commission européenne, saisie par un industriel. Le panel de scientifiques a appuyé son avis sur un dossier fourni par l'industriel lui-même.
L’avis porte sur l’utilisation après séchage des larves de ténébrion (Tenebrio molitor), entières ou sous forme de poudre incluse ensuite dans un aliment. Après récolte des œufs et éclosion, les larves sont élevées dans des containers et nourries de végétaux et de farines de céréales. Au bout de 11 semaines, elles sont tamisées afin d’éliminer tout déchet (substrat, exuvies, fèces, etc.) et triées pour retirer les larves mortes. Elles sont ensuite tuées par un passage pendant 1 à 5 minutes dans de l’eau bouillante, séchées puis déshydratées en four ventilé. Les larves commercialisées entières ou broyées (poudre) sont ensachées et stockées à température ambiante.
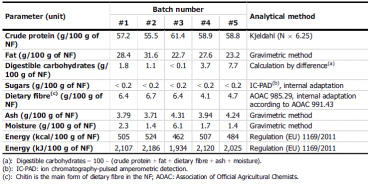
Ce nouvel aliment est proposé pour l’ensemble de la population, sous des formes variées : en-cas et snacking (en particulier pour les larves entières), produits à forte teneur protéique pour les sportifs, ingrédient de biscuits et de produits à base de légumes ou de pâtes. Il se caractérise par sa richesse en protéine, en matières grasses et en fibres (tableau ci-dessous), sous ses deux formes. Le taux protéique élevé doit cependant être relativisé car la technique d’analyse inclut la présence de chitine, composante principale des fibres alimentaires insolubles. Les taux de traces de métaux lourds, de mycotoxines et de bactéries sont inférieurs aux normes recommandées.
Composition de 5 échantillons de larve de ténébrion in toto
Source : Efsa
Notons enfin que ce produit ne présente pas de toxicité particulière. Des allergies, rares, sont cependant possibles et documentées dans les pays asiatiques, consommateurs d’insectes. Un risque d’allergie croisée est possible pour les personnes allergiques aux crustacés et acariens. Les experts rendent donc un avis favorable à ce nouvel aliment pour les usages prévus tout en recommandant à son producteur d’engager des recherches sur son allergénicité.
Franck Bourdy, Centre d'études et de prospective
18:29 Publié dans 4. Politiques publiques, Alimentation et consommation | Lien permanent | Tags : insectes, efsa, sécurité alimentaire, alimentation, novel food, transformation |  Imprimer | |
Imprimer | |  |
| ![]() Facebook
Facebook
06/03/2019
Quel avenir pour les analogues à la viande ? Considérations de Chatham House pour l'Union européenne
Dans un document de travail de Chatham House publié en février 2019, A. Frogatt et L. Wellesley proposent un état des lieux des produits analogues à la viande, aussi bien d'origine végétale que « cultivés » à partir de cellules animales (in vitro) (cf. figure). Innovations, facteurs de développement et implications réglementaires pour l'Union européenne (UE) sont passés en revue. Selon les auteurs, la « viande cultivée » est à l'heure actuelle au stade du prototype, développé par des start-up financées par des grands groupes. Le marché des substituts d'origine végétale reste limité (moins de 1 % du marché de la viande aux États-Unis), mais connaît une croissance significative. Le développement d'un marché des produits analogues à la viande dépendra de plusieurs facteurs : perceptions des consommateurs, bilan environnemental, demande globale de produits carnés, stratégies concurrentes du secteur de la viande « traditionnelle », coûts de production, etc. Dans l'UE, la viande cultivée devrait, pour les auteurs, relever de la réglementation Novel Food, ce qui n'est pas nécessairement le cas pour les produits d'origine végétale. Le document souligne également l'importance de la question des labels, et la nécessité pour l'Union de réfléchir en termes de cadre réglementaire et de stratégie industrielle pour préparer l'avenir.
Procédés de production de la « viande cultivée » et de la « viande d'origine végétale »
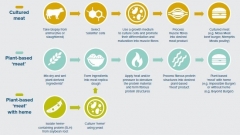
Source : Chatham House
Source : Chatham House
13:08 Publié dans 5. Fait porteur d'avenir | Lien permanent | Tags : viande, viande in vitro, substituts, novel food |  Imprimer | |
Imprimer | |  |
| ![]() Facebook
Facebook
11/12/2015
Évolution réglementaire européenne sur les nouveaux aliments
Le 11 décembre a été publié au Journal officiel de l’Union européenne un nouveau règlement « novel food » qui entrera en vigueur dans deux ans. Par « nouvel aliment », il faut entendre un aliment qui n’était pas consommé de manière significative en Europe avant mai 1997 (date de parution du premier règlement). Il peut s’agir d’aliments innovants produits avec de nouvelles technologies mais constitués d'ingrédients connus (cas des aliments incluant des nanomatériaux), d’aliments produits sur cultures cellulaires ou issus de structures minérales, ou encore d’aliments consommés dans les pays tiers (exemple des insectes) mais non encore consommés habituellement en Europe.
Pour la mise sur le marché de ces denrées, le nouveau texte propose une procédure d’autorisation centralisée : l’industriel dépose le dossier directement à la Direction générale Santé et sécurité sanitaire de la Commission européenne, qui fait procéder à une évaluation par l’Autorité européenne de sécurité des aliments (EFSA). L’objectif est aujourd'hui de raccourcir le temps de traitement du dossier (de l’ordre de deux ans avec la procédure actuelle), de favoriser l’innovation et de garantir une équité dans le traitement des dossiers, une seule agence intervenant ici. Les États membres sont ensuite consultés collégialement avant l’autorisation.
Pour certains produits spécifiques, classés « nouveaux aliments » car non consommés actuellement en Europe, mais faisant l’objet d’une consommation courante dans les pays tiers sans alerte de santé depuis au moins 25 ans, une procédure particulière pourrait être prévue, telle une simple notification. Cette disposition s’appliquerait aux insectes.
Pour mémoire, le règlement « novel food » était en cours de réévaluation depuis plusieurs années, un précédent projet n’avait pu aboutir en 2008 du fait d’absence de consensus sur l’étiquetage des produits issus d’animaux clonés. C’est pourquoi le projet actuel n’inclut pas ces produits qui feront l’objet d’une réglementation à part. Les aliments génétiquement modifiés ne sont pas non plus concernés.
Madeleine Lesage, Centre d’études et de prospective
Sources : Commission européenne, EUR-Lex
10:35 Publié dans 4. Politiques publiques, Santé et risques sanitaires | Lien permanent | Tags : novel food |  Imprimer | |
Imprimer | |  |
| ![]() Facebook
Facebook